2025年成考高起点每日一练《理化综合》4月22日专为备考2025年理化综合考生准备,帮助考生通过每日坚持练习,逐步提升考试成绩。
单选题
1、下列对二氧化硫的叙述错误的是()。
- A:可使品红溶液褪色
- B:既具有氧化性,又具有还原性
- C:是造成酸雨污染环境的主要有害气体之一
- D:溶于水生成硫酸,又叫硫酸酐
答 案:D
解 析:本题A、B、C三个选项都是对二氧化硫的性质及危害的正确描述。二氧化硫是一个重要化合物,所以关于它的物理性质、化学性质及对环境造成的危害等内容,应作为重点掌握。D选项是错误的,因为SO2溶于水生成H2SO3(亚硫酸)。  所以SO2是亚硫酸的酸酐。 SO3溶于水生成H2SO4。
所以SO2是亚硫酸的酸酐。 SO3溶于水生成H2SO4。 所以硫酸的酸酐是SO3。
所以硫酸的酸酐是SO3。
应记住:SO2对应的是亚硫酸(H2SO3)和亚硫酸盐,如Na2SO3;SO3对应的是硫酸(H2SO4)和硫酸盐,如Na2SO4。
2、下列物质中,含有氧分子的是()。
- A:氯酸钾
- B:液氧
- C:二氧化碳
- D:氧化铁
答 案:B
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、工业上用焙烧NaHCO3的方法生产纯碱(Na2CO3)。现有17.5g的NaHCO3样品,加热分解完全后,生成标准状况下的CO2气体2.24L。写出NaHCO3分解反应的化学方程式,计算此NaHCO3样品的纯度。
答 案:NaHCO3分解反应的化学方程式如下: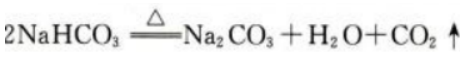 反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
2、一绝缘细绳上端固定,下端连接在一质量m=0.08kg、长度l=0.4m的均匀金属棒中心,整个装置处在一匀强磁场中,磁场的磁感应强度大小B=0.5T,方向竖直向上,如图所示。现使一电流流过金属棒,已知电流大小I=3A,方向垂直于纸面向里,重力加速度大小g取10m/s2。求
(1)金属棒所受安培力的大小和方向。
(2)平衡后细绳中张力的大小及细绳与竖直方向夹角的正切值。
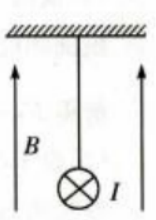
答 案:.(1)金属棒所受安培力为F=BIL=0.6N,根据左手定则知,方向水平向右。 (2)金属棒所受重力为G=mg=0.8N平衡后,安培力与重力的合力与绳中张力等大反向,设细绳与竖直方向的夹角为θ,则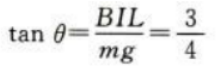 绳中张力大小为
绳中张力大小为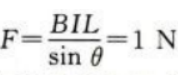
填空题
1、一质点沿x轴运动,其位置随时间变化的图像如图所示。由图可知,质点在1s和4s时的瞬时速度分别为()m/s、()m/s;质点0~6s这段时间内的平均速度为()m/s。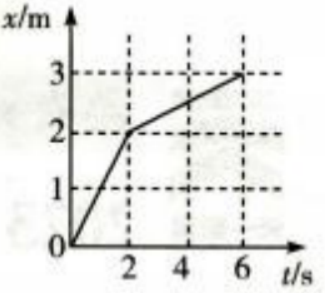
答 案:1;0.25;0.5
解 析:本题考查了瞬时速度、平均速度的知识点。 根据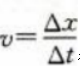 得1s时的速度为1m/s,4s时的速度为0.25m/s,6s内的平均速度为0.5m/s。
得1s时的速度为1m/s,4s时的速度为0.25m/s,6s内的平均速度为0.5m/s。
2、氯化铝溶液滴入烧碱溶液中发生反应的离子方程式为()
答 案: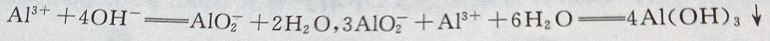
解 析: 溶液滴入烧碱溶液,开始时碱过量,两者发生反应为
溶液滴入烧碱溶液,开始时碱过量,两者发生反应为
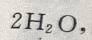 随着
随着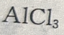 的加入,生成的
的加入,生成的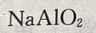 又会与过量的
又会与过量的 溶液反应,
溶液反应,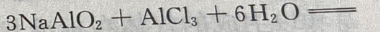

简答题
1、画出硫离子、镁离子、氯离子结构示意图。
答 案: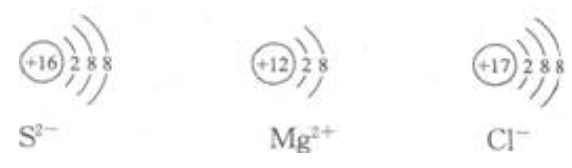
2、如图11-27所示,两根相距0.5m光滑平行金属导轨CE和C’E’放置在水平面上,两端分别连接电阻R1=R2=1Ω,AB的质量m=1kg,匀强磁场的磁感应强度B=0.2T,AB和导轨的电阻忽略不计,今给AB一个初动量,使其以初速度ν0=10m/s在导轨上向右运动,求:(1)AB开始运动时所受的磁场力.
(2)在AB运动过程中,R:上放出的热量.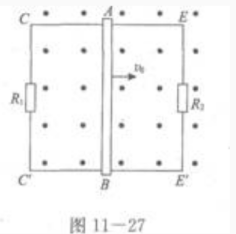
答 案:(1)当AB运动时切割磁感线,产生感应电动势。因此,它相当于一个电源。由图可见,外电路是 R1和R2的并联电路,由右手定则知,金属棒AB中的感应电流由A流向B.再用左手定则知,金属棒AB所受的磁场力F方向向左,与运动方向相反,由此可知,金属棒做减速运动,最后静止不动.当AB以速度v运动时,感应电动势为 因为R1与R2并联,所以电功率与电阻成反比,因此热量与电阻成反比,故有
因为R1与R2并联,所以电功率与电阻成反比,因此热量与电阻成反比,故有

精彩评论