2025年成考高起点每日一练《理化综合》5月22日专为备考2025年理化综合考生准备,帮助考生通过每日坚持练习,逐步提升考试成绩。
单选题
1、某金属M与铜组成原电池时,M为负极,发生氧化反应。锌可从该金属盐溶液中置换出金属M。则金属M是()
- A:Mg
- B:Fe
- C:Al
- D:Ag
答 案:B
解 析:在原电池中,M作负极,说明金属活泼性比正极的Cu强,锌可从该金属的盐溶液中置换出该金属,说明该金属的活泼性比锌弱,符合条件的是铁。
2、质量相同的SO2和SO3,它们中所含氧原子个数之比为()。
- A:4:5
- B:5:4
- C:5:6
- D:2:3
答 案:C
解 析:此题中的关键词是“质量相同”和“氧原子个数”。(1)质量相同的SO2和SO3的物质的量之比:设SO2和SO3质量均为1g,则 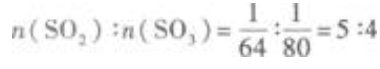 (2)质量相同的SO2和SO3中的氧原子个数之比: n(SO2)×2:n(SO3)x3=5x2:4x3=5:6
(2)质量相同的SO2和SO3中的氧原子个数之比: n(SO2)×2:n(SO3)x3=5x2:4x3=5:6
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
1、工业上用焙烧NaHCO3的方法生产纯碱(Na2CO3)。现有17.5g的NaHCO3样品,加热分解完全后,生成标准状况下的CO2气体2.24L。写出NaHCO3分解反应的化学方程式,计算此NaHCO3样品的纯度。
答 案:NaHCO3分解反应的化学方程式如下: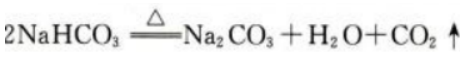 反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
2、如图,一质量为m1的木块静置在光滑的水平面上,一质量为m2的子弹以速度v0水平射入木块,进入木块s距离后相对木块静止。设子弹相对木块静止前受到的阻力恒定。求从子弹开始进入到相对木块静止这段时间内
(1)子弹与木块组成的系统损失的机械能。
(2)木块移动的距离。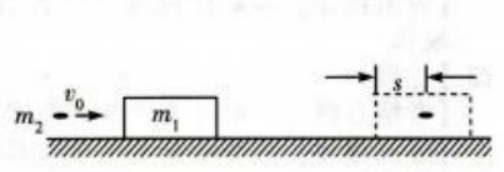
答 案:(1)根据动量守恒定律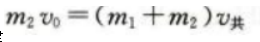 根据功能关系
根据功能关系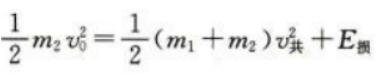
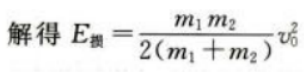 (2)设子弹与木块间摩擦力为f,则E损=fs设物块运动距离为L,对物块运用动能定理
(2)设子弹与木块间摩擦力为f,则E损=fs设物块运动距离为L,对物块运用动能定理
填空题
1、A、B两元素的离子具有相同的电子数,A、B两元素的单质都能与水剧烈反应,在反应中A单质作还原剂,B单质作氧化剂。A与B反应的生成物的电子式为()。
答 案:
解 析:根据题给条件知:在反应中A单质作还原剂则为金属元素,B单质作氧化剂则为非金属。而非金属单质常温下能与水剧烈反应的只有F2,其阴离子为2、8结构。
2、若要除去硫酸亚铁中含有的少量Fe3+和Cu2+,最好加入______。
答 案:铁粉
解 析:除杂质有以下要求: (1)把杂质除去或使其变成能与所需要的有效成分分离开的物质。如此题为除去FeSO4中 的Fe3+和Cu2+,加入铁粉后发生如下反应: 第一个反应把杂质(Fe3+)变成了有效成分(Fe2+),这种结果最好。第二个反应把混在溶液中的Cu2+变成了不溶于水的Cu单质,用过滤法即可与Fe2+分开。
第一个反应把杂质(Fe3+)变成了有效成分(Fe2+),这种结果最好。第二个反应把混在溶液中的Cu2+变成了不溶于水的Cu单质,用过滤法即可与Fe2+分开。
(2)不能引入新杂质。只从与Fe3+、Cu2+反应的角度看,不加铁粉加锌粉也可以。因为加锌粉后,发生如下反应: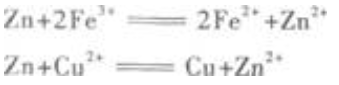 从反应方程式看,的确除去了Fe3+和Cu2+,但却引入了Zn2+,不符合要求。
从反应方程式看,的确除去了Fe3+和Cu2+,但却引入了Zn2+,不符合要求。
简答题
1、如图11—30所示,一台理想变压器,输入电压为220V,输出电压有10V、110V两组线圈,10V的线圈有50匝,输出电流为2A,110V线圈的输出电流为0.5A,求: (1)110V输出线圈的匝数。
(2)输入线圈的匝数。
(3)输入电流。 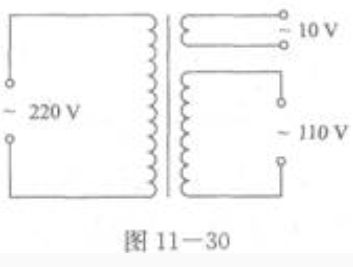
答 案:
2、60kg的物体以2m/s的速度竖直匀速下降,若向上的力突然变为617.4N,并持续2s,求物体在这2s内下降的高度。
答 案:分析物体的受力情况如图3—10所示,取向下的方向为正方向,有:
精彩评论